

การเข้าชม: 0 ผู้แต่ง: บรรณาธิการเว็บไซต์ เวลาเผยแพร่: 30-10-2568 ที่มา: เว็บไซต์









แบเรียมซัลเฟต (BaSO₄) เป็นสารประกอบเคมีที่มีการนำไปใช้งานในวงกว้างทั้งในด้านเคมี อุตสาหกรรม และการแพทย์ BaSO₄ เป็นที่รู้จักในเรื่องสีขาวสว่าง ความหนาแน่นสูง และความเสถียรทางเคมี โดยถูกใช้เป็นสารตัวเติมในพลาสติก เม็ดสีในสี และแม้กระทั่งเป็นสารตัดกันในการถ่ายภาพทางการแพทย์ แม้ว่าจะมีวางจำหน่ายในรูปแบบของแข็ง แต่ลักษณะพื้นฐานที่สุดประการหนึ่งของแบเรียมซัลเฟตในทางเคมีก็คือการก่อตัวเป็นตะกอน การทำความเข้าใจกระบวนการนี้เป็นสิ่งสำคัญสำหรับนักเคมี ผู้ปฏิบัติงานในอุตสาหกรรม และช่างเทคนิคในห้องปฏิบัติการ
ในปฏิกิริยาเคมี ตะกอนหมายถึงของแข็งที่เกิดขึ้นเมื่อสารประกอบที่ละลายน้ำได้ 2 ชนิดทำปฏิกิริยาในสารละลาย การก่อตัวของ BaSO₄ ในฐานะตะกอนมีความหมายที่สำคัญ ตั้งแต่การพิจารณาความเข้มข้นของซัลเฟตในเคมีวิเคราะห์ไปจนถึงการผลิตวัสดุบริสุทธิ์สำหรับใช้ในอุตสาหกรรมและทางการแพทย์ การทราบว่าแบเรียมซัลเฟตก่อให้เกิดตะกอนหรือไม่ช่วยให้นักวิจัยเข้าใจกลไกการเกิดปฏิกิริยา รับประกันคุณภาพของผลิตภัณฑ์ และรักษามาตรฐานความปลอดภัยเมื่อจัดการกับสารประกอบแบเรียม
ตะกอนคือสารของแข็งที่เกิดจากสารละลายระหว่างปฏิกิริยาเคมี ซึ่งมักเป็นผลจากการรวมสารประกอบที่ละลายน้ำได้ 2 ชนิดเข้าด้วยกันทำให้เกิดผลิตภัณฑ์ที่ไม่ละลายน้ำ ต่างจากไอออนละลายที่เคลื่อนที่อย่างอิสระในสารละลาย การตกตะกอนจะก่อตัวเป็นอนุภาคของแข็งที่สามารถตกตะกอนหรือแยกออกได้โดยการกรองหรือการหมุนเหวี่ยง
ปฏิกิริยาการตกตะกอนมีความสำคัญในเคมีวิเคราะห์ การผลิตทางอุตสาหกรรม และการวิจัย ตัวอย่างทั่วไป ได้แก่ ปฏิกิริยาของซิลเวอร์ไนเตรตกับโซเดียมคลอไรด์เพื่อสร้างซิลเวอร์คลอไรด์ (AgCl) และปฏิกิริยาของแคลเซียมคลอไรด์กับโซเดียมคาร์บอเนตเพื่อสร้างแคลเซียมคาร์บอเนต (CaCO₃) ปฏิกิริยาเหล่านี้มีลักษณะพิเศษคือการปรากฏของแข็งอย่างกะทันหันภายในสารละลายใสก่อนหน้านี้
ความสามารถของสารประกอบในการตกตะกอนมักถูกทำนายโดยใช้ค่าคงที่ผลิตภัณฑ์ที่สามารถละลายได้ (Ksp) Ksp กำหนดความเข้มข้นสูงสุดของไอออนที่มีอยู่ในสารละลายโดยไม่เกิดเป็นของแข็ง หากผลิตภัณฑ์ไอออนิกเกินค่านี้ สารละลายจะมีความอิ่มตัวยิ่งยวด และสารประกอบจะตกตะกอน สำหรับแบเรียมซัลเฟต ผลิตภัณฑ์ที่มีความสามารถในการละลายต่ำมาก ซึ่งหมายความว่าแบเรียมและซัลเฟตไอออนในสารละลายมีความเข้มข้นเพียงเล็กน้อยก็สามารถทำให้เกิดการตกตะกอนได้
แบเรียมซัลเฟตมักเกิดขึ้นจากปฏิกิริยาระหว่างเกลือแบเรียมที่ละลายน้ำได้กับเกลือซัลเฟตในสารละลายที่เป็นน้ำ ตัวอย่างเช่น:
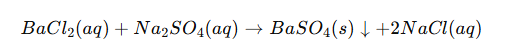
ในทำนองเดียวกัน แบเรียมไนเตรตสามารถทำปฏิกิริยากับกรดซัลฟิวริกหรือโซเดียมซัลเฟตเพื่อสร้างตะกอนแบบเดียวกัน:
![]()
แบเรียมซัลเฟตที่ได้จะเป็นของแข็งเนื้อละเอียดสีขาวและหนาแน่นซึ่งไม่ละลายในน้ำสูง ปฏิกิริยานี้แสดงให้เห็นถึงพฤติกรรมดั้งเดิมของการตกตะกอน เนื่องจากผลิตภัณฑ์แยกออกจากสารละลายทันทีเนื่องจากมีความสามารถในการละลายต่ำมาก
ลักษณะทางกายภาพของตะกอนมีสีขาวสว่าง ความหนาแน่นสูง และขนาดอนุภาคละเอียด ขึ้นอยู่กับสภาวะของปฏิกิริยาและวิธีการเตรียม BaSO₄ อาจปรากฏเป็นไมโครคริสตัลไลน์รวมตัวหรือสารแขวนลอยคอลลอยด์
สารตั้งต้นที่มีความเข้มข้นสูง
สภาพแวดล้อมที่สามารถละลายได้ต่ำ
อุณหภูมิโดยรอบหรือสูงขึ้นเล็กน้อย
ไม่มีการรบกวนไอออนหรือสารก่อเชิงซ้อน
มีหลายปัจจัยที่ส่งผลต่อการก่อตัว ขนาด และคุณภาพของตะกอนแบเรียมซัลเฟต:
อัตราส่วนของแบเรียมไอออนต่อซัลเฟตไอออนจะส่งผลต่อปฏิกิริยาการตกตะกอนโดยสมบูรณ์ ไอออนที่มากเกินไปเล็กน้อยอาจส่งผลต่อขนาดอนุภาคและความสม่ำเสมอของตะกอน ในปฏิกิริยาทางอุตสาหกรรมหรือในห้องปฏิบัติการ ปริมาณสารสัมพันธ์ที่ได้รับการควบคุมอย่างระมัดระวังช่วยให้มั่นใจได้ถึงผลลัพธ์ที่สม่ำเสมอและทำซ้ำได้
แม้ว่า BaSO₄ จะไม่ละลายน้ำสูง แต่อุณหภูมิและองค์ประกอบไอออนิกของสารละลายอาจมีอิทธิพลอย่างละเอียดต่ออัตราการเกิดนิวเคลียสและการเติบโตของผลึก อุณหภูมิที่สูงขึ้นอาจเร่งกระบวนการตกตะกอน ในขณะที่ความแข็งแรงของไอออนิกสูงอาจส่งผลต่อขนาดและการรวมตัวของอนุภาค
สิ่งเจือปนในสารตั้งต้นหรือการมีอยู่ของสารเติมแต่งสามารถยับยั้งการเติบโตของผลึก เปลี่ยนสัณฐานวิทยาของอนุภาค หรือส่งผลต่อการตกตะกอน ในการใช้งานทางอุตสาหกรรมบางประเภท มีการเพิ่มตัวดัดแปลงพื้นผิวเพื่อควบคุมขนาดอนุภาค ป้องกันการจับตัวเป็นก้อน และเพิ่มการกระจายตัวในพลาสติก สารเคลือบ หรือสารแขวนลอยทางการแพทย์

ในห้องปฏิบัติการ สามารถสังเกตและยืนยันการตกตะกอนของแบเรียมซัลเฟตได้โดยใช้เทคนิคต่างๆ:
BaSO₄ ปรากฏเป็นของแข็งสีขาวสว่างทันทีที่ก่อตัว ในสารละลายที่ผสมกันอย่างดี ตะกอนอาจปรากฏเป็นคอลลอยด์และแขวนลอย และตกตะกอนในที่สุดเนื่องจากแรงโน้มถ่วง
นักเคมีใช้การกรองหรือการหมุนเหวี่ยงเพื่อแยกตะกอน การกรองจะจับของแข็งบนตัวกลาง เช่น กระดาษกรองหรือเมมเบรน ในขณะที่การหมุนเหวี่ยงจะช่วยเร่งการตกตะกอนของอนุภาคละเอียดเพื่อการแยกที่ง่ายขึ้น
การวิเคราะห์แบบกราวิเมตริกเป็นวิธีการทั่วไปในการยืนยันการตกตะกอนของ BaSO₄ ในเทคนิคนี้ ตะกอนจะถูกกรอง ทำให้แห้ง และชั่งน้ำหนักเพื่อหาปริมาณซัลเฟตหรือแบเรียมในสารละลายตั้งต้น วิธีการขั้นสูง เช่น การเลี้ยวเบนรังสีเอกซ์ (XRD) หรือกล้องจุลทรรศน์อิเล็กตรอนสามารถเปิดเผยโครงสร้างผลึกและสัณฐานวิทยาของอนุภาคได้ โดยแยกไมโครคริสตัลไลน์ออกจากรูปแบบคอลลอยด์
การตกตะกอนแบเรียมซัลเฟตมีบทบาทสำคัญในการวิเคราะห์ทางห้องปฏิบัติการเชิงปริมาณ ด้วยการสร้างตะกอนที่บริสุทธิ์และเสถียร นักเคมีจึงสามารถระบุความเข้มข้นของซัลเฟตในน้ำ ดิน น้ำทิ้งทางอุตสาหกรรม หรือตัวอย่างทางชีววิทยาได้อย่างแม่นยำ ความสามารถในการละลายต่ำของ BaSO₄ ช่วยให้มั่นใจในความแม่นยำสูงในการตรวจวิเคราะห์แบบกราวิเมตริกและปริมาตร
ในอุตสาหกรรม ตะกอนแบเรียมซัลเฟตถูกนำมาใช้ในหลายวิธี:
การบำบัดน้ำ: การตกตะกอน BaSO₄ ช่วยกำจัดซัลเฟตไอออนออกจากน้ำเสีย ป้องกันการเกิดตะกรันและการปนเปื้อนต่อสิ่งแวดล้อม
การผลิตเม็ดสี: BaSO₄ ที่ตกตะกอนถูกใช้เป็นสารตัวเติมและเม็ดสีในสี สารเคลือบ และพลาสติก เนื่องจากมีความขาว ความเฉื่อยทางเคมี และมีความหนาแน่นสูง
สารตัวเติมโพลีเมอร์: BaSO₄ ช่วยเพิ่มความแข็ง ความมันเงาของพื้นผิว และความคงตัวของมิติในผลิตภัณฑ์พลาสติกและผลิตภัณฑ์ยาง
แม้ว่า BaSO ₄ เกรดเภสัชกรรม ที่ใช้ในการถ่ายภาพเอ็กซ์เรย์ผลิตภายใต้มาตรฐานที่เข้มงวด แนวคิดเรื่องการตกตะกอนมีความเกี่ยวข้อง การตกตะกอนในห้องปฏิบัติการทำให้มั่นใจได้ถึงความบริสุทธิ์สูงและขนาดอนุภาคที่ควบคุมได้ ซึ่งมีความสำคัญอย่างยิ่งต่อการสร้างสารแขวนลอยที่เคลือบระบบทางเดินอาหารได้อย่างปลอดภัยและให้ภาพเอ็กซ์เรย์ที่ชัดเจน อนุภาคที่ละเอียดและสม่ำเสมอของแบบฟอร์มที่ตกตะกอนช่วยป้องกันการจับตัวเป็นก้อนและรับประกันการกระจายตัวที่สม่ำเสมอในตัวกลางคอนทราสต์
สิ่งสำคัญคือต้องชี้แจงความเข้าใจผิดทั่วไปหลายประการเกี่ยวกับ BaSO₄:
ไม่ได้เติมเป็นของแข็งเสมอไป: แม้ว่า BaSO₄ จะมีในรูปของแข็ง แต่ในหลาย ๆ ปฏิกิริยา สารดังกล่าวจะถูกสร้างขึ้นในแหล่งกำเนิดผ่านการตกตะกอน วิธีการนี้ช่วยให้มั่นใจได้ถึงความบริสุทธิ์ที่สูงขึ้นและการควบคุมคุณลักษณะของอนุภาคได้อย่างแม่นยำ
การเปรียบเทียบกับสารประกอบแบเรียมอื่นๆ: เกลือแบเรียมที่ละลายน้ำได้ เช่น แบเรียมคลอไรด์หรือไนเตรต จะไม่ตกตะกอนด้วยตัวเอง แต่จะก่อตัวเป็น BaSO₄ เมื่อรวมกับซัลเฟตไอออน สิ่งนี้ทำให้พวกมันแตกต่างในแง่ของการจัดการและการใช้งานสารเคมี
ความบริสุทธิ์และความสม่ำเสมอ: การตกตะกอนช่วยให้แน่ใจว่า BaSO₄ ปราศจากสิ่งปนเปื้อนที่ละลายได้ ทำให้เหมาะสำหรับวัตถุประสงค์ในการวิเคราะห์ อุตสาหกรรม และทางการแพทย์
การทำความเข้าใจการตกตะกอนของแบเรียมซัลเฟตมีประโยชน์มากมาย:
ความแม่นยำในการทดลองที่ได้รับการปรับปรุง: การก่อตัวของ BaSO₄ บริสุทธิ์ที่คาดการณ์ได้ ช่วยให้สามารถตรวจวัดแบบกราวิเมตริกและเชิงวิเคราะห์ได้อย่างแม่นยำ
ประสิทธิภาพทางอุตสาหกรรมที่ปรับให้เหมาะสม: การตกตะกอนที่มีการควบคุมทำให้มั่นใจได้ว่าขนาดอนุภาคจะสม่ำเสมอ ซึ่งมีความสำคัญอย่างยิ่งต่อสารตัวเติม สารเคลือบ และพลาสติก
การจัดการที่ปลอดภัยยิ่งขึ้น: BaSO₄ ที่ตกตะกอนไม่ละลายน้ำและไม่เป็นพิษ ซึ่งช่วยลดความเสี่ยงที่เกี่ยวข้องกับสารประกอบแบเรียมที่ละลายได้
ความสม่ำเสมอในการใช้งานทางการแพทย์: ขนาดอนุภาคที่สม่ำเสมอในสารคอนทราสต์ของรังสีเอกซ์ทำให้มั่นใจได้ถึงผลลัพธ์การถ่ายภาพที่เชื่อถือได้
คำถามที่ 1: เมื่อ BaSO₄ ตกตะกอนหมายความว่าอย่างไร
หมายความว่าแบเรียมไอออนและซัลเฟตไอออนในสารละลายรวมกันเป็นสารประกอบที่เป็นของแข็งและไม่ละลายน้ำซึ่งแยกออกจากของเหลว
คำถามที่ 2: เกลือแบเรียมทั้งหมดสามารถเกิดการตกตะกอนด้วยซัลเฟตไอออนได้หรือไม่
เกลือแบเรียมที่ละลายได้ส่วนใหญ่ เช่น แบเรียมคลอไรด์และแบเรียมไนเตรต จะก่อให้เกิดตะกอน BaSO₄ เมื่อรวมกับเกลือซัลเฟต
คำถามที่ 3: แบเรียมซัลเฟตตกตะกอนในสารละลายได้เร็วแค่ไหน?
การตกตะกอนจะเกิดขึ้นเกือบจะในทันทีเมื่อมีการผสมสารละลายที่มีแบเรียมและซัลเฟตไอออนที่มีความเข้มข้นเพียงพอ
คำถามที่ 4: ตะกอนสามารถนำมาใช้โดยตรงในงานอุตสาหกรรมได้หรือไม่?
ได้ BaSO₄ ที่ตกตะกอนสามารถนำไปแปรรูปและใช้เป็นสารตัวเติม เม็ดสี หรือในการใช้งานอื่นๆ ได้ ขึ้นอยู่กับขนาดอนุภาคและความบริสุทธิ์
คำถามที่ 5: BaSO₄ ที่ตกตะกอนแตกต่างจากแบไรท์ธรรมชาติอย่างไร
แบไรท์ธรรมชาติถูกขุดขึ้นมาและมักต้องมีการทำให้บริสุทธิ์ BaSO₄ ที่ตกตะกอนถูกสร้างขึ้นในสภาวะที่มีการควบคุม ส่งผลให้มีความบริสุทธิ์สูงขึ้นและขนาดอนุภาคสม่ำเสมอ
แบเรียมซัลเฟต เป็นตัวอย่างคลาสสิกของการตกตะกอน ซึ่งเกิดขึ้นเมื่อเกลือแบเรียมที่ละลายน้ำได้ทำปฏิกิริยากับซัลเฟตไอออน ความไม่ละลายน้ำ ความคงตัวทางเคมี และคุณลักษณะของอนุภาคละเอียด ทำให้มีความสำคัญในการวิเคราะห์ในห้องปฏิบัติการ การผลิตทางอุตสาหกรรม และการใช้งานทางการแพทย์ รวมถึงการถ่ายภาพรังสีเอกซ์ การทำความเข้าใจกระบวนการตกตะกอนทำให้มั่นใจได้ว่าผลลัพธ์ BaSO₄ มีความบริสุทธิ์สูง แสดงให้เห็นประสิทธิภาพที่สม่ำเสมอ และสามารถจัดการได้อย่างปลอดภัยในสภาพแวดล้อมต่างๆ
สำหรับมืออาชีพและอุตสาหกรรมที่กำลังมองหาแบเรียมซัลเฟตที่เชื่อถือได้และมีคุณภาพสูง การเป็นพันธมิตรกับซัพพลายเออร์ที่มีชื่อเสียงถือเป็นสิ่งสำคัญ Qingdao Red Butterfly Precision Materials Co., Ltd. นำเสนอ BaSO₄ ที่ได้รับการประมวลผลอย่างระมัดระวังด้วยขนาดอนุภาคที่ควบคุมได้และความบริสุทธิ์ทางเคมีที่เหนือกว่า ทำให้เหมาะสำหรับวัตถุประสงค์ในการวิเคราะห์ อุตสาหกรรม และทางการแพทย์ ด้วยการจัดหาจากซัพพลายเออร์ที่เชื่อถือได้ ผู้ใช้จะได้รับผลลัพธ์ที่ดีที่สุดในการทดลอง กระบวนการผลิต และการใช้งานด้านการวินิจฉัย ในขณะเดียวกันก็ลดความเสี่ยงของการปนเปื้อนหรือประสิทธิภาพที่ไม่สอดคล้องกัน การติดต่อบริษัทโดยตรงทำให้สามารถเข้าถึงคำแนะนำจากผู้เชี่ยวชาญ เกรดที่กำหนดเอง และการสนับสนุนผลิตภัณฑ์ที่เชื่อถือได้สำหรับข้อกำหนดแบเรียมซัลเฟต
