

Visualizações: 0 Autor: Editor do site Horário de publicação: 30/10/2025 Origem: Site









O sulfato de bário (BaSO₄) é um composto químico com amplas aplicações na química, indústria e medicina. Conhecido por sua cor branca brilhante, alta densidade e estabilidade química, o BaSO₄ é usado como enchimento em plásticos, pigmentos em tintas e até mesmo como agente de contraste em imagens médicas. Embora esteja comercialmente disponível na forma sólida, um dos aspectos mais fundamentais do sulfato de bário na química é a sua formação como precipitado. Compreender este processo é fundamental para químicos, operadores industriais e técnicos de laboratório.
Nas reações químicas, um precipitado refere-se a um sólido que se forma quando dois compostos solúveis reagem em solução. A formação de O BaSO₄ como precipitado tem implicações importantes, desde a determinação das concentrações de sulfato na química analítica até a produção de materiais puros para uso industrial e médico. Saber se o sulfato de bário forma um precipitado ajuda os pesquisadores a compreender os mecanismos de reação, garantir a qualidade do produto e manter os padrões de segurança ao manusear compostos de bário.
Um precipitado é uma substância sólida que emerge de uma solução durante uma reação química, geralmente como resultado da combinação de dois compostos solúveis que produzem um produto insolúvel. Ao contrário dos íons dissolvidos que se movem livremente na solução, os precipitados agregam-se para formar partículas sólidas que podem sedimentar ou ser separadas por filtração ou centrifugação.
As reações de precipitação são essenciais na química analítica, na fabricação industrial e na pesquisa. Exemplos comuns incluem a reação do nitrato de prata com cloreto de sódio para formar cloreto de prata (AgCl) e a reação do cloreto de cálcio com carbonato de sódio para formar carbonato de cálcio (CaCO₃). Estas reações são caracterizadas pelo aparecimento repentino de um sólido dentro de uma solução previamente límpida.
A capacidade de precipitação de um composto é frequentemente prevista usando sua constante de produto de solubilidade (Ksp). O Ksp define a concentração máxima de íons que pode existir em solução sem formar um sólido. Se o produto iônico exceder esse valor, a solução fica supersaturada e o composto precipita. Para o sulfato de bário, o produto de solubilidade é extremamente baixo, o que significa que mesmo pequenas concentrações de íons bário e sulfato em solução podem levar à precipitação.
O sulfato de bário é mais comumente formado através de uma reação entre um sal de bário solúvel e um sal de sulfato em solução aquosa. Por exemplo:
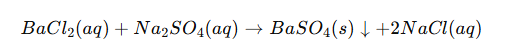
Da mesma forma, o nitrato de bário pode reagir com ácido sulfúrico ou sulfato de sódio para produzir o mesmo precipitado:
![]()
O sulfato de bário resultante é um sólido fino, branco e denso, altamente insolúvel em água. Esta reação demonstra o comportamento clássico da precipitação, pois o produto se separa imediatamente da solução devido à sua baixíssima solubilidade.
As características físicas do precipitado incluem cor branca brilhante, alta densidade e tamanho de partícula fino. Dependendo das condições de reação e do método de preparação, o BaSO4 pode aparecer como agregados microcristalinos ou como uma suspensão coloidal.
Alta concentração de reagentes
Ambientes de baixa solubilidade
Temperaturas ambientes ou ligeiramente elevadas
Ausência de íons interferentes ou agentes complexantes
Vários fatores afetam a formação, tamanho e qualidade do precipitado de sulfato de bário:
A proporção de íons de bário para íons de sulfato influencia o quão completamente ocorre a reação de precipitação. Um ligeiro excesso de qualquer um dos íons pode afetar o tamanho das partículas e a homogeneidade do precipitado. Em reações em escala industrial ou de laboratório, a estequiometria cuidadosamente controlada garante resultados consistentes e reprodutíveis.
Embora o BaSO₄ seja altamente insolúvel, a temperatura e a composição iônica da solução podem influenciar sutilmente a taxa de nucleação e o crescimento do cristal. Temperaturas mais altas podem acelerar o processo de precipitação, enquanto a alta força iônica pode impactar o tamanho e a agregação das partículas.
As impurezas nos reagentes, ou a presença de aditivos, podem inibir o crescimento do cristal, alterar a morfologia das partículas ou afetar a sedimentação. Em algumas aplicações industriais, modificadores de superfície são adicionados para controlar o tamanho das partículas, evitar aglomeração e aumentar a dispersibilidade em plásticos, revestimentos ou suspensões médicas.

Em laboratório, a precipitação de sulfato de bário pode ser observada e confirmada usando múltiplas técnicas:
BaSO4 aparece como um sólido branco brilhante imediatamente após a formação. Em soluções bem misturadas, o precipitado pode parecer coloidal e suspenso, eventualmente sedimentando devido à gravidade.
Para isolar o precipitado, os químicos usam filtração ou centrifugação. A filtração captura o sólido em um meio, como papel de filtro ou membrana, enquanto a centrifugação acelera a sedimentação de partículas finas para facilitar a separação.
A análise gravimétrica é um método comum para confirmar a precipitação de BaSO₄. Nesta técnica, o precipitado é filtrado, seco e pesado para determinar a quantidade de sulfato ou bário na solução original. Métodos avançados como difração de raios X (XRD) ou microscopia eletrônica podem revelar a estrutura cristalina e a morfologia das partículas, distinguindo as formas microcristalinas das coloidais.
A precipitação com sulfato de bário desempenha um papel crucial na análise laboratorial quantitativa. Ao formar um precipitado puro e estável, os químicos podem determinar com precisão as concentrações de sulfato na água, solo, efluentes industriais ou amostras biológicas. A baixa solubilidade do BaSO₄ garante alta precisão em ensaios gravimétricos e volumétricos.
Na indústria, os precipitados de sulfato de bário são utilizados de diversas maneiras:
Tratamento de Água: A precipitação de BaSO₄ ajuda a remover íons sulfato das águas residuais, evitando a formação de incrustações e a contaminação ambiental.
Produção de pigmentos: O BaSO₄ precipitado é usado como carga e pigmento em tintas, revestimentos e plásticos devido à sua brancura, inércia química e alta densidade.
Cargas de polímero: BaSO₄ melhora a dureza, o brilho da superfície e a estabilidade dimensional em plásticos e produtos de borracha.
Embora O BaSO ₄ de grau farmacêutico usado em imagens de raios X é produzido sob padrões rígidos, o conceito de precipitação é relevante. A precipitação laboratorial garante alta pureza e tamanho de partícula controlado, fundamental para a criação de suspensões que revestem o trato gastrointestinal com segurança e fornecem imagens radiográficas nítidas. As partículas finas e uniformes da forma precipitada ajudam a prevenir a aglomeração e garantem uma distribuição uniforme no meio de contraste.
É importante esclarecer vários equívocos comuns em relação ao BaSO₄:
Nem sempre adicionado como sólido: Embora o BaSO₄ esteja disponível como sólido, em muitas reações ele é gerado in situ por meio de precipitação. Esta abordagem garante maior pureza e controle preciso sobre as características das partículas.
Comparação com outros compostos de bário: Os sais solúveis de bário, como cloreto ou nitrato de bário, não precipitam por si próprios, mas formam BaSO₄ quando combinados com íons sulfato. Isso os distingue em termos de manuseio e aplicações de produtos químicos.
Pureza e consistência: A precipitação garante que o BaSO₄ esteja livre de contaminantes solúveis, tornando-o ideal para fins analíticos, industriais e médicos.
Compreender a precipitação do sulfato de bário oferece inúmeros benefícios:
Precisão Experimental Melhorada: A formação previsível de BaSO₄ puro permite medições gravimétricas e analíticas precisas.
Desempenho Industrial Otimizado: A precipitação controlada garante tamanho de partícula uniforme, fundamental para cargas, revestimentos e plásticos.
Manuseio mais seguro: O BaSO₄ precipitado é insolúvel e não tóxico, reduzindo o risco associado a compostos solúveis de bário.
Consistência em aplicações médicas: O tamanho uniforme das partículas em agentes de contraste de raios X garante resultados de imagem confiáveis.
Q1: O que significa quando o BaSO₄ precipita?
Isso significa que os íons bário e os íons sulfato em solução se combinaram para formar um composto sólido e insolúvel que se separa do líquido.
Q2: Todos os sais de bário podem formar um precipitado com íons sulfato?
A maioria dos sais de bário solúveis, como cloreto de bário e nitrato de bário, formarão um precipitado de BaSO₄ quando combinados com sais de sulfato.
Q3: Com que rapidez o sulfato de bário precipita em solução?
A precipitação ocorre quase imediatamente após a mistura de soluções contendo concentrações suficientes de íons bário e sulfato.
Q4: O precipitado pode ser usado diretamente em aplicações industriais?
Sim, o BaSO₄ precipitado pode ser processado e usado como carga, pigmento ou em outras aplicações, dependendo do tamanho e da pureza da partícula.
Q5: Como o BaSO₄ precipitado difere da barita natural?
A barita natural é extraída e muitas vezes requer purificação. O BaSO₄ precipitado é gerado em condições controladas, resultando em maior pureza e tamanho de partícula uniforme.
O sulfato de bário é um exemplo clássico de precipitado, formado quando sais solúveis de bário reagem com íons sulfato. Sua insolubilidade, estabilidade química e características de partículas finas o tornam essencial em análises laboratoriais, fabricação industrial e aplicações médicas, incluindo imagens de raios X. A compreensão do processo de precipitação garante que o BaSO₄ resultante seja de alta pureza, apresente desempenho consistente e possa ser manuseado com segurança em vários ambientes.
Para profissionais e indústrias que buscam sulfato de bário confiável e de alta qualidade, é fundamental fazer parceria com um fornecedor confiável. Qingdao Red Butterfly Precision Materials Co., Ltd. oferece BaSO₄ cuidadosamente processado com tamanho de partícula controlado e pureza química superior, tornando-o adequado para fins analíticos, industriais e médicos. Ao adquirir produtos de um fornecedor confiável, os usuários podem obter resultados ideais em experimentos, processos de fabricação e aplicações de diagnóstico, ao mesmo tempo em que minimizam o risco de contaminação ou desempenho inconsistente. Entrar em contato diretamente com a empresa fornece acesso a orientação especializada, classificações personalizadas e suporte confiável ao produto para qualquer necessidade de sulfato de bário.
