

Vues : 0 Auteur : Éditeur du site Heure de publication : 2025-10-30 Origine : Site









Le sulfate de baryum (BaSO₄) est un composé chimique ayant de nombreuses applications dans les domaines de la chimie, de l'industrie et de la médecine. Connu pour sa couleur blanche brillante, sa haute densité et sa stabilité chimique, BaSO₄ est utilisé comme charge dans les plastiques, comme pigment dans les peintures et même comme agent de contraste en imagerie médicale. Bien qu’il soit disponible dans le commerce sous forme solide, l’un des aspects les plus fondamentaux du sulfate de baryum en chimie est sa formation sous forme de précipité. Comprendre ce processus est essentiel pour les chimistes, les opérateurs industriels et les techniciens de laboratoire.
Dans les réactions chimiques, un précipité fait référence à un solide qui se forme lorsque deux composés solubles réagissent en solution. La formation de BaSO₄ en tant que précipité a des implications importantes, depuis la détermination des concentrations de sulfate en chimie analytique jusqu'à la production de matériaux purs à usage industriel et médical. Savoir si le sulfate de baryum forme un précipité aide les chercheurs à comprendre les mécanismes de réaction, à garantir la qualité des produits et à maintenir les normes de sécurité lors de la manipulation des composés de baryum.
Un précipité est une substance solide qui émerge d'une solution lors d'une réaction chimique, souvent à la suite de la combinaison de deux composés solubles qui produisent un produit insoluble. Contrairement aux ions dissous qui se déplacent librement dans la solution, les précipités s'agrègent pour former des particules solides qui peuvent se déposer ou être séparées par filtration ou centrifugation.
Les réactions de précipitation sont essentielles en chimie analytique, en fabrication industrielle et en recherche. Des exemples courants incluent la réaction du nitrate d'argent avec du chlorure de sodium pour former du chlorure d'argent (AgCl) et la réaction du chlorure de calcium avec du carbonate de sodium pour former du carbonate de calcium (CaCO₃). Ces réactions se caractérisent par l’apparition soudaine d’un solide au sein d’une solution auparavant claire.
La capacité d'un composé à précipiter est souvent prédite à l'aide de sa constante de produit de solubilité (Ksp). Le Ksp définit la concentration maximale d'ions pouvant exister en solution sans former de solide. Si le produit ionique dépasse cette valeur, la solution devient sursaturée et le composé précipite. Pour le sulfate de baryum, le produit de solubilité est extrêmement faible, ce qui signifie que même de petites concentrations d’ions baryum et sulfate en solution peuvent conduire à une précipitation.
Le sulfate de baryum se forme le plus souvent par une réaction entre un sel de baryum soluble et un sel sulfate en solution aqueuse. Par exemple:
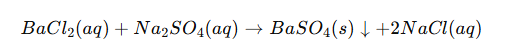
De même, le nitrate de baryum peut réagir avec l'acide sulfurique ou le sulfate de sodium pour produire le même précipité :
![]()
Le sulfate de baryum obtenu est un solide fin, blanc et dense, hautement insoluble dans l’eau. Cette réaction démontre le comportement classique de précipitation, puisque le produit se sépare immédiatement de la solution en raison de sa solubilité extrêmement faible.
Les caractéristiques physiques du précipité comprennent une couleur blanche brillante, une densité élevée et une granulométrie fine. Selon les conditions de réaction et la méthode de préparation, BaSO₄ peut apparaître sous forme d'agrégats microcristallins ou de suspension colloïdale.
Forte concentration de réactifs
Environnements à faible solubilité
Températures ambiantes ou légèrement élevées
Absence d'ions interférents ou d'agents complexants
Plusieurs facteurs affectent la formation, la taille et la qualité du précipité de sulfate de baryum :
Le rapport entre les ions baryum et les ions sulfate influence l’ampleur de la réaction de précipitation. Un léger excès de l’un ou l’autre des ions peut affecter la taille des particules et l’homogénéité du précipité. Dans les réactions industrielles ou à l’échelle du laboratoire, une stœchiométrie soigneusement contrôlée garantit des résultats cohérents et reproductibles.
Bien que BaSO₄ soit hautement insoluble, la température et la composition ionique de la solution peuvent influencer subtilement le taux de nucléation et la croissance cristalline. Des températures plus élevées peuvent accélérer le processus de précipitation, tandis qu'une force ionique élevée peut avoir un impact sur la taille et l'agrégation des particules.
Les impuretés présentes dans les réactifs ou la présence d'additifs peuvent inhiber la croissance des cristaux, modifier la morphologie des particules ou affecter la sédimentation. Dans certaines applications industrielles, des modificateurs de surface sont ajoutés pour contrôler la taille des particules, empêcher l'agglomération et améliorer la dispersibilité dans les plastiques, les revêtements ou les suspensions médicales.

En laboratoire, la précipitation du sulfate de baryum peut être observée et confirmée à l’aide de plusieurs techniques :
BaSO₄ apparaît sous la forme d'un solide blanc brillant immédiatement après sa formation. Dans des solutions bien mélangées, le précipité peut apparaître colloïdal et en suspension, pour finalement se déposer sous l'effet de la gravité.
Pour isoler le précipité, les chimistes utilisent la filtration ou la centrifugation. La filtration capture le solide sur un support, tel qu'un papier filtre ou une membrane, tandis que la centrifugation accélère la décantation des particules fines pour une séparation plus facile.
L'analyse gravimétrique est une méthode courante pour confirmer la précipitation de BaSO₄. Dans cette technique, le précipité est filtré, séché et pesé pour déterminer la quantité de sulfate ou de baryum dans la solution originale. Des méthodes avancées telles que la diffraction des rayons X (DRX) ou la microscopie électronique peuvent révéler la structure cristalline et la morphologie des particules, distinguant ainsi les formes microcristallines des formes colloïdales.
La précipitation du sulfate de baryum joue un rôle crucial dans les analyses quantitatives en laboratoire. En formant un précipité pur et stable, les chimistes peuvent déterminer avec précision les concentrations de sulfate dans l'eau, le sol, les effluents industriels ou les échantillons biologiques. La faible solubilité du BaSO₄ garantit une haute précision dans les analyses gravimétriques et volumétriques.
Dans l'industrie, les précipités de sulfate de baryum sont utilisés de plusieurs manières :
Traitement de l'eau : la précipitation du BaSO₄ aide à éliminer les ions sulfate des eaux usées, empêchant ainsi la formation de tartre et la contamination de l'environnement.
Production de pigments : le BaSO₄ précipité est utilisé comme charge et pigment dans les peintures, les revêtements et les plastiques en raison de sa blancheur, de son inertie chimique et de sa haute densité.
Charges polymères : BaSO₄ améliore la dureté, la brillance de la surface et la stabilité dimensionnelle des produits en plastique et en caoutchouc.
Bien que Le BaSO ₄ de qualité pharmaceutique utilisé en imagerie par rayons X est produit selon des normes strictes, la notion de précipitation est pertinente. La précipitation en laboratoire garantit une pureté élevée et une taille de particule contrôlée, essentielles pour créer des suspensions qui recouvrent le tractus gastro-intestinal en toute sécurité et fournissent des images radiographiques claires. Les particules fines et uniformes de la forme précipitée aident à prévenir l'agglutination et assurent une répartition uniforme dans le produit de contraste.
Il est important de clarifier plusieurs idées fausses courantes concernant BaSO₄ :
Pas toujours ajouté sous forme solide : Bien que BaSO₄ soit disponible sous forme solide, dans de nombreuses réactions, il est généré in situ par précipitation. Cette approche garantit une plus grande pureté et un contrôle précis des caractéristiques des particules.
Comparaison avec d'autres composés de baryum : les sels de baryum solubles, comme le chlorure ou le nitrate de baryum, ne précipitent pas d'eux-mêmes mais forment du BaSO₄ lorsqu'ils sont combinés avec des ions sulfate. Cela les distingue en termes de manipulation et d’applications de produits chimiques.
Pureté et cohérence : la précipitation garantit que BaSO₄ est exempt de contaminants solubles, ce qui le rend idéal à des fins analytiques, industrielles et médicales.
Comprendre la précipitation du sulfate de baryum offre de nombreux avantages :
Précision expérimentale améliorée : la formation prévisible de BaSO₄ pur permet des mesures gravimétriques et analytiques précises.
Performance industrielle optimisée : les précipitations contrôlées garantissent une taille de particule uniforme, essentielle pour les charges, les revêtements et les plastiques.
Manipulation plus sûre : le BaSO₄ précipité est insoluble et non toxique, ce qui réduit le risque associé aux composés de baryum solubles.
Cohérence dans les applications médicales : la taille uniforme des particules dans les agents de contraste pour rayons X garantit des résultats d'imagerie fiables.
Q1 : Qu'est-ce que cela signifie lorsque BaSO₄ précipite ?
Cela signifie que les ions baryum et les ions sulfate en solution se sont combinés pour former un composé solide et insoluble qui se sépare du liquide.
Q2 : Tous les sels de baryum peuvent-ils former un précipité avec les ions sulfate ?
La plupart des sels de baryum solubles, tels que le chlorure de baryum et le nitrate de baryum, formeront un précipité BaSO₄ lorsqu'ils seront combinés avec des sels de sulfate.
Q3 : À quelle vitesse le sulfate de baryum précipite-t-il en solution ?
La précipitation se produit presque immédiatement lors du mélange de solutions contenant des concentrations suffisantes d'ions baryum et sulfate.
Q4 : Le précipité peut-il être utilisé directement dans des applications industrielles ?
Oui, le BaSO₄ précipité peut être traité et utilisé comme charge, pigment ou dans d'autres applications, en fonction de la taille et de la pureté des particules.
Q5 : En quoi le BaSO₄ précipité est-il différent de la barytine naturelle ?
La barytine naturelle est extraite et nécessite souvent une purification. Le BaSO₄ précipité est généré dans des conditions contrôlées, ce qui entraîne une pureté plus élevée et une taille de particule uniforme.
Le sulfate de baryum est un exemple classique de précipité formé lorsque des sels de baryum solubles réagissent avec des ions sulfate. Son insolubilité, sa stabilité chimique et ses caractéristiques de particules fines le rendent essentiel dans les analyses de laboratoire, la fabrication industrielle et les applications médicales, y compris l'imagerie par rayons X. Comprendre le processus de précipitation garantit que le BaSO₄ résultant est d'une grande pureté, présente des performances constantes et peut être manipulé en toute sécurité dans divers contextes.
Pour les professionnels et les industries à la recherche de sulfate de baryum fiable et de haute qualité, un partenariat avec un fournisseur réputé est essentiel. Qingdao Red Butterfly Precision Materials Co., Ltd. propose du BaSO₄ soigneusement traité avec une granulométrie contrôlée et une pureté chimique supérieure, ce qui le rend adapté à des fins analytiques, industrielles et médicales. En s'approvisionnant auprès d'un fournisseur de confiance, les utilisateurs peuvent obtenir des résultats optimaux dans les expériences, les processus de fabrication et les applications de diagnostic, tout en minimisant le risque de contamination ou de performances incohérentes. Contacter directement l'entreprise donne accès à des conseils d'experts, à des qualités personnalisées et à une assistance produit fiable pour tout besoin en sulfate de baryum.
