

Aufrufe: 0 Autor: Site-Editor Veröffentlichungszeit: 30.10.2025 Herkunft: Website









Bariumsulfat (BaSO₄) ist eine chemische Verbindung mit vielfältigen Anwendungen in der Chemie, Industrie und Medizin. BaSO₄ ist für seine strahlend weiße Farbe, hohe Dichte und chemische Stabilität bekannt und wird als Füllstoff in Kunststoffen, Pigmente in Farben und sogar als Kontrastmittel in der medizinischen Bildgebung verwendet. Während es im Handel in fester Form erhältlich ist, ist die Bildung eines Niederschlags einer der grundlegendsten Aspekte von Bariumsulfat in der Chemie. Das Verständnis dieses Prozesses ist für Chemiker, Industriebetreiber und Labortechniker gleichermaßen von entscheidender Bedeutung.
Bei chemischen Reaktionen bezeichnet ein Niederschlag einen Feststoff, der entsteht, wenn zwei lösliche Verbindungen in Lösung reagieren. Die Bildung von BaSO₄ als Niederschlag hat wichtige Auswirkungen, von der Bestimmung von Sulfatkonzentrationen in der analytischen Chemie bis hin zur Herstellung reiner Materialien für industrielle und medizinische Zwecke. Zu wissen, ob Bariumsulfat einen Niederschlag bildet, hilft Forschern, Reaktionsmechanismen zu verstehen, die Produktqualität sicherzustellen und Sicherheitsstandards beim Umgang mit Bariumverbindungen einzuhalten.
Ein Niederschlag ist eine feste Substanz, die während einer chemischen Reaktion aus einer Lösung austritt, oft als Ergebnis der Kombination zweier löslicher Verbindungen, die ein unlösliches Produkt erzeugen. Im Gegensatz zu gelösten Ionen, die sich in der Lösung frei bewegen, aggregieren Niederschläge zu festen Partikeln, die sich absetzen oder durch Filtration oder Zentrifugation abgetrennt werden können.
Fällungsreaktionen sind in der analytischen Chemie, der industriellen Fertigung und Forschung von wesentlicher Bedeutung. Gängige Beispiele sind die Reaktion von Silbernitrat mit Natriumchlorid zur Bildung von Silberchlorid (AgCl) und die Reaktion von Calciumchlorid mit Natriumcarbonat zur Bildung von Calciumcarbonat (CaCO₃). Diese Reaktionen sind durch das plötzliche Auftreten eines Feststoffs in einer zuvor klaren Lösung gekennzeichnet.
Die Fähigkeit einer Verbindung zur Ausfällung wird oft anhand ihrer Löslichkeitsproduktkonstante (Ksp) vorhergesagt. Der Ksp definiert die maximale Ionenkonzentration, die in Lösung existieren kann, ohne einen Feststoff zu bilden. Übersteigt das ionische Produkt diesen Wert, wird die Lösung übersättigt und die Verbindung fällt aus. Für Bariumsulfat ist das Löslichkeitsprodukt extrem niedrig, was bedeutet, dass bereits geringe Konzentrationen von Barium- und Sulfationen in Lösung zu Ausfällungen führen können.
Bariumsulfat entsteht am häufigsten durch eine Reaktion zwischen einem löslichen Bariumsalz und einem Sulfatsalz in wässriger Lösung. Zum Beispiel:
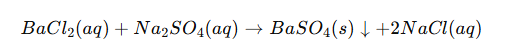
Ebenso kann Bariumnitrat mit Schwefelsäure oder Natriumsulfat reagieren und denselben Niederschlag erzeugen:
![]()
Das resultierende Bariumsulfat ist ein feiner, weißer, dichter Feststoff, der in Wasser kaum löslich ist. Diese Reaktion zeigt das klassische Verhalten der Fällung, da sich das Produkt aufgrund seiner extrem geringen Löslichkeit sofort aus der Lösung trennt.
Zu den physikalischen Eigenschaften des Niederschlags gehören eine strahlend weiße Farbe, eine hohe Dichte und eine feine Partikelgröße. Abhängig von den Reaktionsbedingungen und der Herstellungsmethode kann BaSO₄ als mikrokristalline Aggregate oder als kolloidale Suspension auftreten.
Hohe Konzentration an Reaktanten
Umgebungen mit geringer Löslichkeit
Umgebungstemperatur oder leicht erhöhte Temperatur
Keine störenden Ionen oder Komplexbildner
Mehrere Faktoren beeinflussen die Bildung, Größe und Qualität des Bariumsulfat-Niederschlags:
Das Verhältnis von Bariumionen zu Sulfationen beeinflusst, wie vollständig die Fällungsreaktion abläuft. Ein leichter Überschuss an einem der beiden Ionen kann die Partikelgröße und Homogenität des Niederschlags beeinträchtigen. Bei Reaktionen im Industrie- oder Labormaßstab sorgt eine sorgfältig kontrollierte Stöchiometrie für konsistente und reproduzierbare Ergebnisse.
Obwohl BaSO₄ sehr unlöslich ist, können die Temperatur und die ionische Zusammensetzung der Lösung die Keimbildungsrate und das Kristallwachstum geringfügig beeinflussen. Höhere Temperaturen können den Fällungsprozess beschleunigen, während eine hohe Ionenstärke die Größe und Aggregation der Partikel beeinflussen kann.
Verunreinigungen in den Reaktanten oder das Vorhandensein von Zusatzstoffen können das Kristallwachstum hemmen, die Partikelmorphologie verändern oder die Sedimentation beeinflussen. In einigen industriellen Anwendungen werden Oberflächenmodifikatoren zugesetzt, um die Partikelgröße zu kontrollieren, die Agglomeration zu verhindern und die Dispergierbarkeit in Kunststoffen, Beschichtungen oder medizinischen Suspensionen zu verbessern.

In einer Laborumgebung kann die Ausfällung von Bariumsulfat mithilfe mehrerer Techniken beobachtet und bestätigt werden:
BaSO₄ erscheint unmittelbar nach der Bildung als hellweißer Feststoff. In gut gemischten Lösungen kann der Niederschlag kolloidal und suspendiert erscheinen und sich schließlich aufgrund der Schwerkraft absetzen.
Um den Niederschlag zu isolieren, nutzen Chemiker Filtration oder Zentrifugation. Durch die Filtration wird der Feststoff auf einem Medium wie Filterpapier oder einer Membran aufgefangen, während die Zentrifugation das Absetzen feiner Partikel beschleunigt und so die Trennung erleichtert.
Die gravimetrische Analyse ist eine gängige Methode zur Bestätigung der BaSO₄-Ausfällung. Bei dieser Technik wird der Niederschlag filtriert, getrocknet und gewogen, um die Menge an Sulfat oder Barium in der ursprünglichen Lösung zu bestimmen. Fortschrittliche Methoden wie Röntgenbeugung (XRD) oder Elektronenmikroskopie können die kristalline Struktur und Partikelmorphologie aufdecken und mikrokristalline von kolloidalen Formen unterscheiden.
Die Fällung von Bariumsulfat spielt in der quantitativen Laboranalytik eine entscheidende Rolle. Durch die Bildung eines reinen, stabilen Niederschlags können Chemiker die Sulfatkonzentrationen in Wasser, Boden, Industrieabwässern oder biologischen Proben genau bestimmen. Die geringe Löslichkeit von BaSO₄ gewährleistet eine hohe Präzision bei gravimetrischen und volumetrischen Untersuchungen.
In der Industrie werden Bariumsulfat-Niederschläge auf verschiedene Arten genutzt:
Wasseraufbereitung: Die BaSO₄-Fällung trägt dazu bei, Sulfationen aus dem Abwasser zu entfernen und so Kalkablagerungen und Umweltverschmutzung zu verhindern.
Pigmentherstellung: Ausgefälltes BaSO₄ wird aufgrund seines Weißgrades, seiner chemischen Inertheit und seiner hohen Dichte als Füllstoff und Pigment in Farben, Beschichtungen und Kunststoffen verwendet.
Polymerfüllstoffe: BaSO₄ verbessert die Härte, den Oberflächenglanz und die Dimensionsstabilität in Kunststoffen und Gummiprodukten.
Obwohl Da BaSO₄ in pharmazeutischer Qualität, das in der Röntgenbildgebung verwendet wird, unter strengen Standards hergestellt wird, ist das Konzept der Ausfällung relevant. Die Laborfällung gewährleistet eine hohe Reinheit und kontrollierte Partikelgröße, was für die Herstellung von Suspensionen, die den Magen-Darm-Trakt sicher bedecken und klare Röntgenbilder liefern, von entscheidender Bedeutung ist. Die feinen, gleichmäßigen Partikel der ausgefällten Form verhindern eine Verklumpung und sorgen für eine gleichmäßige Verteilung im Kontrastmittel.
Es ist wichtig, einige häufige Missverständnisse in Bezug auf BaSO₄ zu klären:
Nicht immer als Feststoff zugesetzt: Während BaSO₄ als Feststoff vorliegt, wird es bei vielen Reaktionen in situ durch Fällung erzeugt. Dieser Ansatz gewährleistet eine höhere Reinheit und eine präzise Kontrolle der Partikeleigenschaften.
Vergleich mit anderen Bariumverbindungen: Lösliche Bariumsalze wie Bariumchlorid oder -nitrat fallen nicht von selbst aus, sondern bilden in Kombination mit Sulfationen BaSO₄. Dies zeichnet sie hinsichtlich der Handhabung und Anwendung von Chemikalien aus.
Reinheit und Konsistenz: Die Fällung stellt sicher, dass BaSO₄ frei von löslichen Verunreinigungen ist, was es ideal für analytische, industrielle und medizinische Zwecke macht.
Das Verständnis der Ausfällung von Bariumsulfat bietet zahlreiche Vorteile:
Verbesserte experimentelle Genauigkeit: Die vorhersagbare Bildung von reinem BaSO₄ ermöglicht präzise gravimetrische und analytische Messungen.
Optimierte industrielle Leistung: Die kontrollierte Ausfällung sorgt für eine gleichmäßige Partikelgröße, die für Füllstoffe, Beschichtungen und Kunststoffe entscheidend ist.
Sicherere Handhabung: Ausgefälltes BaSO₄ ist unlöslich und ungiftig, wodurch das mit löslichen Bariumverbindungen verbundene Risiko verringert wird.
Konsistenz in medizinischen Anwendungen: Eine einheitliche Partikelgröße in Röntgenkontrastmitteln sorgt für zuverlässige Bildergebnisse.
F1: Was bedeutet es, wenn BaSO₄ ausfällt?
Dies bedeutet, dass sich Bariumionen und Sulfationen in Lösung zu einer festen, unlöslichen Verbindung verbunden haben, die sich von der Flüssigkeit trennt.
F2: Können alle Bariumsalze mit Sulfationen einen Niederschlag bilden?
Die meisten löslichen Bariumsalze wie Bariumchlorid und Bariumnitrat bilden in Kombination mit Sulfatsalzen einen BaSO₄-Niederschlag.
F3: Wie schnell fällt Bariumsulfat in Lösung aus?
Beim Mischen von Lösungen, die ausreichende Konzentrationen an Barium- und Sulfationen enthalten, kommt es fast sofort zur Ausfällung.
F4: Kann der Niederschlag direkt in industriellen Anwendungen verwendet werden?
Ja, ausgefälltes BaSO₄ kann je nach Partikelgröße und Reinheit verarbeitet und als Füllstoff, Pigment oder in anderen Anwendungen verwendet werden.
F5: Wie unterscheidet sich ausgefälltes BaSO₄ von natürlichem Baryt?
Natürlicher Baryt wird abgebaut und erfordert häufig eine Reinigung. Ausgefälltes BaSO₄ wird unter kontrollierten Bedingungen erzeugt, was zu höherer Reinheit und einheitlicher Partikelgröße führt.
Bariumsulfat ist ein klassisches Beispiel für einen Niederschlag, der entsteht, wenn lösliche Bariumsalze mit Sulfationen reagieren. Aufgrund seiner Unlöslichkeit, chemischen Stabilität und Feinpartikeleigenschaften ist es unverzichtbar für Laboranalysen, industrielle Fertigung und medizinische Anwendungen, einschließlich Röntgenbildgebung. Das Verständnis des Fällungsprozesses stellt sicher, dass das resultierende BaSO₄ von hoher Reinheit ist, eine konstante Leistung aufweist und in verschiedenen Umgebungen sicher gehandhabt werden kann.
Für Fachleute und Branchen, die zuverlässiges, qualitativ hochwertiges Bariumsulfat suchen, ist die Partnerschaft mit einem seriösen Lieferanten von entscheidender Bedeutung. Qingdao Red Butterfly Precision Materials Co., Ltd. bietet sorgfältig verarbeitetes BaSO₄ mit kontrollierter Partikelgröße und hervorragender chemischer Reinheit, wodurch es für analytische, industrielle und medizinische Zwecke geeignet ist. Durch die Beschaffung bei einem vertrauenswürdigen Lieferanten können Benutzer optimale Ergebnisse bei Experimenten, Herstellungsprozessen und Diagnoseanwendungen erzielen und gleichzeitig das Risiko einer Kontamination oder inkonsistenter Leistung minimieren. Wenn Sie sich direkt an das Unternehmen wenden, erhalten Sie Zugang zu fachkundiger Beratung, maßgeschneiderten Qualitäten und zuverlässigem Produktsupport für alle Anforderungen an Bariumsulfat.
