

Vistas: 0 Autor: Editor del sitio Hora de publicación: 2025-10-30 Origen: Sitio









El sulfato de bario (BaSO₄) es un compuesto químico con una amplia gama de aplicaciones en la química, la industria y la medicina. Conocido por su color blanco brillante, alta densidad y estabilidad química, el BaSO₄ se utiliza como relleno en plásticos, pigmentos en pinturas e incluso como agente de contraste en imágenes médicas. Si bien está disponible comercialmente en forma sólida, uno de los aspectos más fundamentales del sulfato de bario en química es su formación como precipitado. Comprender este proceso es fundamental tanto para químicos, operadores industriales y técnicos de laboratorio.
En reacciones químicas, un precipitado se refiere a un sólido que se forma cuando dos compuestos solubles reaccionan en solución. la formación de El BaSO₄ como precipitado tiene implicaciones importantes, desde la determinación de concentraciones de sulfato en química analítica hasta la producción de materiales puros para uso industrial y médico. Saber si el sulfato de bario forma un precipitado ayuda a los investigadores a comprender los mecanismos de reacción, garantizar la calidad del producto y mantener los estándares de seguridad al manipular compuestos de bario.
Un precipitado es una sustancia sólida que emerge de una solución durante una reacción química, a menudo como resultado de la combinación de dos compuestos solubles que producen un producto insoluble. A diferencia de los iones disueltos que se mueven libremente en la solución, los agregados precipitan para formar partículas sólidas que pueden sedimentarse o separarse mediante filtración o centrifugación.
Las reacciones de precipitación son esenciales en la química analítica, la fabricación industrial y la investigación. Los ejemplos comunes incluyen la reacción del nitrato de plata con cloruro de sodio para formar cloruro de plata (AgCl) y la reacción del cloruro de calcio con carbonato de sodio para formar carbonato de calcio (CaCO₃). Estas reacciones se caracterizan por la aparición repentina de un sólido dentro de una solución previamente clara.
La capacidad de un compuesto para precipitar a menudo se predice utilizando su constante de producto de solubilidad (Ksp). La Ksp define la concentración máxima de iones que pueden existir en solución sin formar un sólido. Si el producto iónico excede este valor, la solución se sobresatura y el compuesto precipita. Para el sulfato de bario, el producto de solubilidad es extremadamente bajo, lo que significa que incluso pequeñas concentraciones de iones de bario y sulfato en solución pueden provocar precipitación.
El sulfato de bario se forma más comúnmente mediante una reacción entre una sal de bario soluble y una sal de sulfato en solución acuosa. Por ejemplo:
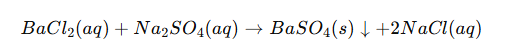
De manera similar, el nitrato de bario puede reaccionar con ácido sulfúrico o sulfato de sodio para producir el mismo precipitado:
![]()
El sulfato de bario resultante es un sólido fino, blanco y denso que es altamente insoluble en agua. Esta reacción demuestra el comportamiento clásico de la precipitación, ya que el producto se separa inmediatamente de la solución debido a su extremadamente baja solubilidad.
Las características físicas del precipitado incluyen un color blanco brillante, alta densidad y tamaño de partícula fino. Dependiendo de las condiciones de la reacción y del método de preparación, el BaSO₄ puede aparecer como agregados microcristalinos o una suspensión coloidal.
Alta concentración de reactivos.
Ambientes de baja solubilidad
Temperaturas ambiente o ligeramente elevadas.
Ausencia de iones que interfieren o agentes complejantes.
Varios factores afectan la formación, el tamaño y la calidad del precipitado de sulfato de bario:
La proporción de iones de bario a iones de sulfato influye en la intensidad de la reacción de precipitación. Un ligero exceso de cualquiera de los iones puede afectar el tamaño de las partículas y la homogeneidad del precipitado. En reacciones industriales o a escala de laboratorio, la estequiometría cuidadosamente controlada garantiza resultados consistentes y reproducibles.
Aunque el BaSO₄ es altamente insoluble, la temperatura y la composición iónica de la solución pueden influir sutilmente en la velocidad de nucleación y crecimiento de los cristales. Las temperaturas más altas pueden acelerar el proceso de precipitación, mientras que la alta fuerza iónica puede afectar el tamaño y la agregación de las partículas.
Las impurezas en los reactivos o la presencia de aditivos pueden inhibir el crecimiento de los cristales, cambiar la morfología de las partículas o afectar la sedimentación. En algunas aplicaciones industriales, se agregan modificadores de superficie para controlar el tamaño de las partículas, evitar la aglomeración y mejorar la dispersabilidad en plásticos, recubrimientos o suspensiones médicas.

En un laboratorio, la precipitación de sulfato de bario se puede observar y confirmar mediante múltiples técnicas:
BaSO₄ aparece como un sólido blanco brillante inmediatamente después de su formación. En soluciones bien mezcladas, el precipitado puede aparecer coloidal y suspendido, y eventualmente sedimentarse debido a la gravedad.
Para aislar el precipitado, los químicos utilizan filtración o centrifugación. La filtración captura el sólido en un medio, como papel de filtro o membrana, mientras que la centrifugación acelera la sedimentación de partículas finas para facilitar la separación.
El análisis gravimétrico es un método común para confirmar la precipitación de BaSO₄. En esta técnica, el precipitado se filtra, se seca y se pesa para determinar la cantidad de sulfato o bario en la solución original. Los métodos avanzados como la difracción de rayos X (DRX) o la microscopía electrónica pueden revelar la estructura cristalina y la morfología de las partículas, distinguiendo las formas microcristalinas de las coloidales.
La precipitación de sulfato de bario juega un papel crucial en el análisis cuantitativo de laboratorio. Al formar un precipitado puro y estable, los químicos pueden determinar con precisión las concentraciones de sulfato en el agua, el suelo, los efluentes industriales o las muestras biológicas. La baja solubilidad del BaSO₄ garantiza una alta precisión en ensayos gravimétricos y volumétricos.
En la industria, los precipitados de sulfato de bario se utilizan de varias formas:
Tratamiento del agua: la precipitación de BaSO₄ ayuda a eliminar los iones de sulfato de las aguas residuales, previniendo la formación de incrustaciones y la contaminación ambiental.
Producción de pigmentos: El BaSO₄ precipitado se utiliza como relleno y pigmento en pinturas, revestimientos y plásticos debido a su blancura, inercia química y alta densidad.
Rellenos poliméricos: BaSO₄ mejora la dureza, el brillo de la superficie y la estabilidad dimensional en productos de plástico y caucho.
A pesar de El BaSO₄ de calidad farmacéutica utilizado en la obtención de imágenes de rayos X se produce bajo estándares estrictos, el concepto de precipitación es relevante. La precipitación en el laboratorio garantiza una alta pureza y un tamaño de partícula controlado, fundamental para crear suspensiones que recubran el tracto gastrointestinal de forma segura y proporcionen imágenes radiográficas claras. Las partículas finas y uniformes de la forma precipitada ayudan a prevenir la formación de grumos y garantizan una distribución uniforme en los medios de contraste.
Es importante aclarar varios conceptos erróneos comunes sobre el BaSO₄:
No siempre se agrega como sólido: si bien el BaSO₄ está disponible como sólido, en muchas reacciones se genera in situ mediante precipitación. Este enfoque garantiza una mayor pureza y un control preciso sobre las características de las partículas.
Comparación con otros compuestos de bario: las sales de bario solubles, como el cloruro o el nitrato de bario, no precipitan por sí solas, sino que forman BaSO₄ cuando se combinan con iones de sulfato. Esto los distingue en términos de manipulación y aplicaciones químicas.
Pureza y consistencia: la precipitación garantiza que BaSO₄ esté libre de contaminantes solubles, lo que lo hace ideal para fines analíticos, industriales y médicos.
Comprender la precipitación del sulfato de bario ofrece numerosos beneficios:
Precisión experimental mejorada: la formación predecible de BaSO₄ puro permite mediciones gravimétricas y analíticas precisas.
Rendimiento industrial optimizado: la precipitación controlada garantiza un tamaño de partícula uniforme, fundamental para rellenos, revestimientos y plásticos.
Manipulación más segura: El BaSO₄ precipitado no es soluble ni tóxico, lo que reduce el riesgo asociado con los compuestos de bario solubles.
Consistencia en aplicaciones médicas: el tamaño uniforme de las partículas en los agentes de contraste para rayos X garantiza resultados de imágenes confiables.
P1: ¿Qué significa cuando precipita BaSO₄?
Significa que los iones de bario y los iones de sulfato en solución se han combinado para formar un compuesto sólido e insoluble que se separa del líquido.
P2: ¿Todas las sales de bario pueden formar un precipitado con iones sulfato?
La mayoría de las sales de bario solubles, como el cloruro de bario y el nitrato de bario, formarán un precipitado de BaSO₄ cuando se combinan con sales de sulfato.
P3: ¿Qué tan rápido precipita el sulfato de bario en solución?
La precipitación ocurre casi inmediatamente al mezclar soluciones que contienen concentraciones suficientes de iones de bario y sulfato.
P4: ¿Se puede utilizar el precipitado directamente en aplicaciones industriales?
Sí, el BaSO₄ precipitado se puede procesar y utilizar como relleno, pigmento o en otras aplicaciones, según el tamaño de las partículas y la pureza.
P5: ¿En qué se diferencia el BaSO₄ precipitado de la barita natural?
La barita natural se extrae y a menudo requiere purificación. El BaSO₄ precipitado se genera en condiciones controladas, lo que da como resultado una mayor pureza y un tamaño de partícula uniforme.
El sulfato de bario es un ejemplo clásico de precipitado, que se forma cuando las sales de bario solubles reaccionan con iones de sulfato. Su insolubilidad, estabilidad química y características de partículas finas lo hacen esencial en análisis de laboratorio, fabricación industrial y aplicaciones médicas, incluidas las imágenes de rayos X. Comprender el proceso de precipitación garantiza que el BaSO₄ resultante sea de alta pureza, muestre un rendimiento constante y pueda manipularse de forma segura en diversos entornos.
Para los profesionales y las industrias que buscan sulfato de bario confiable y de alta calidad, asociarse con un proveedor confiable es fundamental. Qingdao Red Butterfly Precision Materials Co., Ltd. ofrece BaSO₄ cuidadosamente procesado con un tamaño de partícula controlado y una pureza química superior, lo que lo hace adecuado para fines analíticos, industriales y médicos. Al abastecerse de un proveedor confiable, los usuarios pueden lograr resultados óptimos en experimentos, procesos de fabricación y aplicaciones de diagnóstico, al tiempo que minimizan el riesgo de contaminación o rendimiento inconsistente. Ponerse en contacto directamente con la empresa brinda acceso a orientación experta, grados personalizados y soporte confiable de productos para cualquier requisito de sulfato de bario.
